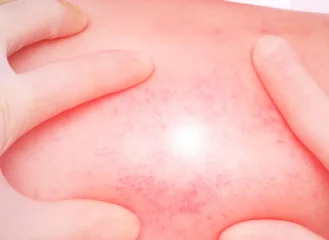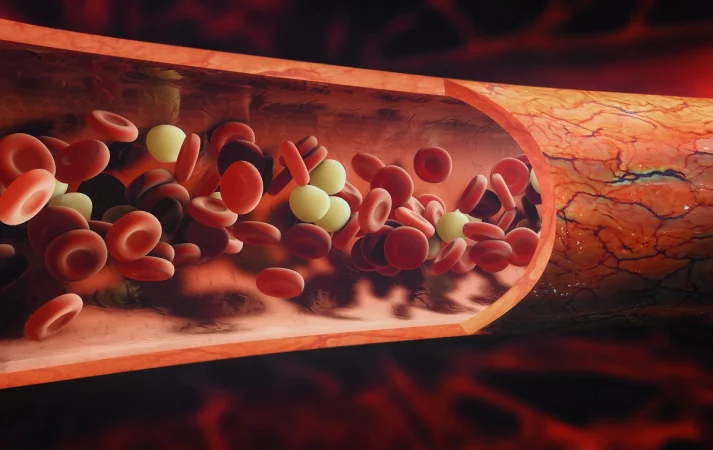
Trombofíliák- genetikai átok, ami trombózist okozhat
A mélyvénás trombózis kialakulásának egyik fő rizikófaktora a genetikai hajlam. Amennyiben valamilyen mutáció következtében van jelen a fokozott hajlam, úgy trombofíliáról beszélünk, melynek több típusa is ismert. Hogy melyek ezek közül a leggyakoribbak, és hogy milyen veszélyeket rejtenek, arról prof. Blaskó György, a Trombózisközpont véralvadási specialistája beszélt.
Mi az a trombofília?
Trombofíliának nevezzük azon állapotokat, melyek a genetikának „köszönhetően” megnövelik a trombózishajlamot. Ennek során a vérzékenység és a véralvadás egyensúlya felborul, méghozzá az utóbbi irányába. Nagy veszélye, hogy ekkor fokozottabban van jelen a vérrögképződés kockázata, ami mélyvénás trombózishoz, esetleg életveszélyes tüdőembóliához vezethet. A trombofíliáknak több formájuk is van, és ezek közül is léteznek súlyos és kevésbé súlyos típusok. Ezek általában már fiatal korban trombózis okoznak, vagy szokatlan helyen keletkező trombózishoz vezetnek.
„40 éve még csak egyetlen trombofiliát ismertünk (az antithrombin nevű fehérje kóros változatát), ma már a genetikai defektusok száma ennek sokszorosa. Mivel általában egy, a genetikai anyagban bekövetkezett változás (mutáció) okoz az illető fehérjében funkcióváltozást, ezeknek alapvetően több típusa van: a) vagy az illető fehérje szintézise csökken, b) vagy olyan mutáció következik be, ami az illető fehérje működését alapjaiban módosítja (pl. nehezebben bomlik, nincs hatása stb). Ily módon ma már a molekuláris defektusok száma a trombózis rendszerében közel 100-ra tehető. Elnevezésünk általában a felfedezés helyével kapcsolat (. pl Factor V Leiden, fibrinogen New York, de van antitrombin-III Budapest és Protein C Pécs is…) Ezeket, azonban csak részletes molekuláris biológiai vizsgálatok segítségével állapíthatjuk meg: a tudományunk jelenleg ott tart, hogy az összes fiatalkori örökletes gyanított trombózis 60-65 %-ában ki tudjuk mutatni a molekuláris hibát. Ez azonban nem jelenti azt, hogy a fennmaradó 40 %-ot ne kezeljük, sőt!”- mondja prof. Blaskó György.
A leggyakoribb trombofíliák
Leiden mutáció
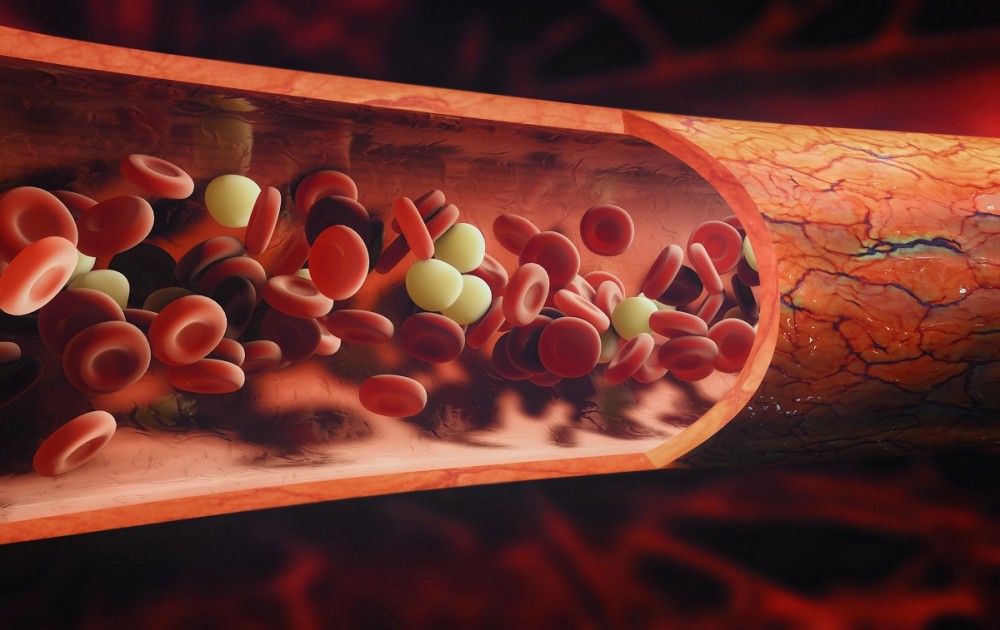 A Leiden mutáció az egyik legismertebb trombofília, így a genetikai vizsgálatok során a legtöbben kérik ennek ellenőrzését (bár a legnagyobb biztonság érdekében általános trombofília szűrést érdemes végeztetni, nem csupán 1-2 mutáció meglétét). Az állapot során a véralvadási rendszer V-ös faktorában egy aminosav-csere van jelen, és ennek következtében a vérrögök kialakulásában nagy szerepet játszó V-ös faktort az azt lebontó enzim (APC) nem képes lebontani. A Leiden mutációnak létezik heterozigóta és homozigóta formája, attól függően, hogy csak az egyik, vagy mindkét szülőtől öröklődött a zavar. A homozigóta forma jóval veszélyesebb, ugyanis megléte akár 80-szorosára is megnövelheti a trombózis kialakulásának rizikóját. Heterozigóta típus esetén az esetek többségében elég a fokozottabb odafigyelés (pl. mozgás, bő folyadékfogyasztás, egészséges életmód), ám ha valaki homozigóta, akkor gyakran véralvadásgátló terápiában kell részesülnie, főleg akkor, ha volt már trombózisa. (Ellenben, ha terhes lesz, a heterozigóta forma is komolyan veendő!)
A Leiden mutáció az egyik legismertebb trombofília, így a genetikai vizsgálatok során a legtöbben kérik ennek ellenőrzését (bár a legnagyobb biztonság érdekében általános trombofília szűrést érdemes végeztetni, nem csupán 1-2 mutáció meglétét). Az állapot során a véralvadási rendszer V-ös faktorában egy aminosav-csere van jelen, és ennek következtében a vérrögök kialakulásában nagy szerepet játszó V-ös faktort az azt lebontó enzim (APC) nem képes lebontani. A Leiden mutációnak létezik heterozigóta és homozigóta formája, attól függően, hogy csak az egyik, vagy mindkét szülőtől öröklődött a zavar. A homozigóta forma jóval veszélyesebb, ugyanis megléte akár 80-szorosára is megnövelheti a trombózis kialakulásának rizikóját. Heterozigóta típus esetén az esetek többségében elég a fokozottabb odafigyelés (pl. mozgás, bő folyadékfogyasztás, egészséges életmód), ám ha valaki homozigóta, akkor gyakran véralvadásgátló terápiában kell részesülnie, főleg akkor, ha volt már trombózisa. (Ellenben, ha terhes lesz, a heterozigóta forma is komolyan veendő!)
Természetesen, hogy kinél szükséges antikoaguláns terápia, azt befolyásolja többek között az, hogy volt-e, és ha igen, akkor mikor, trombózisa, vannak-e egyéb olyan állapotok, melyek megnövelik a rizikót (pl. terhesség, gipsz, túlsúly, diabetes), illetve hogy fennáll-e még más trombofília is mellette - mondja prof. Blaskó György, a Trombózisközpont véralvadási specialistája.
MTHFR mutáció
Az MTHFR mutáció a statisztikák szerint a leggyakrabban előforduló trombofília. A mutáció esetén két helyen is aminosav-csere történik az un. metiltetrahidrofolát reduktáz enzim fehérjében. Maga az MTHFR a folsav-anyagcsere egyik fő eleme, és a mivel a folsavra nagy szükség van a homocisztein lebontásához (a magas homocisztein szint fokozza a vérrög-képződést), így az MTHFR zavara közvetett mód megnöveli a trombózis rizikóját. Akárcsak a Leiden mutációnak, ennek is van hetero-és homozigóta formája. Ez előbbi igen gyakori, a népesség kb. 40 %-ánál fellelhető, ám mivel nem jár nagy homocisztein szint emelkedéssel, és igen ritkán okoz közvetlenül trombózist, így nem veszélyes. Ellentétben homozigóta típus esetén a homocisztein mennyisége lényegesen emelkedett, így ekkor a folsav-pótláson túl sok esetben (pl. terhességkor, ill. korábbi trombózis esetén) véralvadásgátló terápiára van szükség.
Protein S/C alacsony szintje
A Protein S/C szintén fontos szerepet tölt be a véralvadás-vérzékenység egyensúlyában – pontosabban a véralvadással ellentétes fibrinolízisben- ugyanis segítségükkel képes az az aktívált Protein C (APC) a véralvadásban részt vevő faktorokat (V-ös, VIII-as faktort) lebontani. Amennyiben kevés mennyiségben vannak jelen, illetve, ha valamilyen molekuláris defektusuk van, úgy nagyobb a vérrög-képződés esélye. A probléma lehet öröklött és szerzett is (pl. K-vitamin hiány, májbetegség, rosszindulatú daganat, vesebetegség).
Kevés antithrombin
A máj által termelt antithrombin az egyik legfontosabb szerepet játssza a véralvadási folyamatok gátlásában, és ahogy a neve is mutatja, inaktiválja a thrombint és több másik alvadási faktort. Amennyiben túl kevés van belőle, úgy nincs ami ellensúlyozná a véralvadást, így megnő a vérrögök képződésének esélye. Szintén lehet öröklött és szerzett formája is (pl. májbetegség).
Természetesen a fentieken kívül számos más formája is létezik a trombofiliáknak, és bár támogatás nincs rá, az érintett családok tagjait, valamint ez élsportolókat ki kellene vizsgálni ebből a szempontból, és akkor kevesebb lenne a pálya melletti tragédia- tanácsolja a professzor.
Foglaljon időpontot orvosainkhoz!
Téma szakértői
Kapcsolódó oldalak
Páciensek mondták
Magas szakmai színvonal
Nagyon elégedett vagyok. A professzor úr magas szakmai színvonalon kezel évek óta. A beteg felé: humánus, segítőkész , kedves, őszinte. Mind emberileg, mint szakmailag teljesen elkötelezett.